Survey on Machine Learning-based Radiogenomic Study of Breast Cancer
-
摘要:
影像基因组学是一种将基因组数据与成像特征关联的高通量研究方法, 现已广泛应用到乳腺癌分子亚型的鉴别、癌症风险的评估等方面。基于机器学习和大数据技术的影像基因组学在乳腺癌的个性化诊断和治疗等方面都显示出巨大的潜力, 因此, 对机器学习技术在乳腺癌影像基因组学中的研究现状和应用前景进行了总结。首先, 介绍乳腺癌的基因特征和乳腺癌影像数据获取方法, 分析机器学习技术在乳腺癌良性/恶性预测方面的应用; 然后, 对比应用于乳腺癌影像分割问题的深度学习方法, 并分析乳腺癌影像基因组学模型; 最后, 指出当前研究的局限性以及乳腺癌影像基因组学进一步的研究方向。
Abstract:Radiogenomics is a high-throughput research method that correlates genomic data with imaging features, and is now applied widely to the identification of molecular subtypes of breast cancer and the assessment of cancer risk. Radiogenomics, based on machine learning and big data technologies, has shown tremendous potential in personalized diagnosis and treatment of breast cancer. To summarize the current research status and future prospects of machine learning technology in breast cancer radiogenomics, the genetic characteristics of breast cancer and the methods for obtaining breast cancer imaging data were first introduced, and the application of machine learning technology in predicting the benign/malignant nature of breast cancer was analyzed. Subsequently, deep learning methods applied to breast cancer image segmentation problems were compared and breast cancer radiogenomics models were analyzed. Finally, the current limitations of research and further research directions in breast cancer radiogenomics were pointed out.
-
Keywords:
- breast cancer /
- genomics /
- radiomics /
- radiogenomics /
- machine learning /
- image features
-
乳腺癌严重威胁女性的生命和健康,是全球女性最常见的恶性肿瘤[1]。根据CA: A Cancer Journal for Clinicians发布的最新癌症统计报告,2022年美国将有191.8万例新发癌症病例和60.9万癌症病例死亡,其中290 560例为新发乳腺癌病例[2]。中国将会有大约482万新的癌症病例和321万癌症死亡病例,其中大约429 105例为新的乳腺癌病例[3]。乳腺癌仍然是威胁妇女健康的主要癌症之一。了解乳腺癌的发病机理,制定乳腺癌筛查和治疗方法,仍然是保护妇女健康的重要课题。
基因表达谱分析在探究疾病根源上起着重要作用,但通过基因表达谱分析技术对有创的病理组织进行表征分析仅能获得肿瘤的局部信息,不能保证分析结果的准确性和代表性[4-5]。以超声影像为代表的无创影像分析技术克服了以上不足,通过医疗影像可提高人们对肿瘤的整体认识,但很多临床医生很难发现图像中所包含的全部信息,例如肿瘤的纹理特征、直方图特征等。因此,急需一种自动化的技术帮助临床医生提取医疗影像所包含的丰富信息。
影像基因组学的提出进一步提高了人们对肿瘤生物学的认识,可通过建立基因与影像特征之间的关联模型优化临床上的决策[6-7]。目前,肿瘤的影像基因组学研究也面临着诸多挑战,如肿瘤影像展示出的肿瘤形态、纹理等特征与基因之间的关系还不明确,肿瘤病灶的全自动识别与分割难度较大,大多数研究仍是基于兴趣区域(region of interest,ROI)的方式提取特征,缺少统一规范的特征选择标准[8]。
尽管如此,基于机器学习的癌症影像基因组学研究在未来仍具有广阔的发展空间[9]。目前,人工智能被广泛应用于医学影像辅助诊断(简称AI医学影像诊断)[10],尤其在智能影像识别、智能辅助个性化诊断、人机交互辅助诊断、精准治疗辅助决策等方面起到核心支撑作用[11-14]。乳腺癌影像基因组学研究旨在从生物大数据和医学影像大数据中提取出有价值的信息,将其转化为可以量化的数据,用于指导癌症诊断、预后评估、治疗反应预测和疾病状态监测等[15-16]。因此,本文将通过详细地总结和分析近年来基于机器学习的乳腺癌影像基因组学的研究方法和存在的问题探索未来的研究方向,为研究者提供相关研究思路。
1. 影像基因组学
影像基因组学(又称放射基因组学)是一门将医学成像技术与基因组学技术相结合的交叉学科[17],研究目的在于将基因数据和影像数据中有价值的信息转化成医学知识,用于指导癌症检测、诊断、预后评估及治疗反应预测。
基因组学主要对生物体内所有基因进行量化表示,用于指导疾病的诊断与治疗。基因组学包括基因组测序和分析,利用基因测序可以找出癌症的突变基因,从而快速确定对应药物,节省患者诊断时间,提升治疗效果。另外,测序样本只需要患者的血液或唾液,无须传统的病理切片,可以有效减少诊断过程中对患者机体的损伤,但基因测序价格昂贵且操作复杂,使得基因测序很难广泛地应用到临床诊断。随着医学影像技术的快速发展,计算机断层扫描(computerized tomography, CT)、动态对比增强磁共振成像(dynamic contrast-enhanced magnetic resonance imaging, DCE-MRI)、正电子发射体层成像(positron emission tomography, PET)等设备不断地被应用于临床诊断,临床医生可以从视觉上观察患者病灶区域的形态特征,但诊断结果易受医生主观判断的影响。因此,2012年Lambin等[18]提出了影像组学(radiomics)的概念,同年Kumar等[19]又对影像组学的定义进行了拓展。影像组学是指从CT、PET或磁共振成像(magnetic resonance imaging, MRI)等医学设备中获得影像图像,然后高通量地提取并分析大量高级且定量的影像学特征,将图像转换为可挖掘的数据特征,对得到的数据进行分析,以对临床决策提供支持。随着研究的深入发展,很多研究人员发现影像特征与基因型具有多种关联性[20-22],另外,影像基因组学具备医学成像的无创、廉价、可重复的特点,同时也具有利用分子技术直接探索疾病根源的优势,因此,影像基因组学受到广泛关注[23]。其处理流程一般分为5个阶段[24]:数据的收集和预处理、特征提取、特征的选择、模型的建立、模型的临床应用。
2. 乳腺癌基因组学研究
2.1 乳腺癌基因组数据及预处理方法
乳腺癌的基因组特征可分为易感基因突变和单核苷酸多态性(single nucleotide polymorphism, SNP)特征、表达谱特征和分子亚型特征[25]。目前,乳腺癌基因组学分析时常见的表达谱特征包括信使核糖核酸(messenger ribonucleic acid, mRNA)、微小核糖核酸(micro ribonucleic acid, microRNA)、长非编码核糖核酸(long non-coding ribonucleic acid, lncRNA)、拷贝数变异(copy number variation, CNV)、突变数据、蛋白质数据、脱氧核糖核酸(deoxyribonucleic acid, DNA)甲基化等。对数据进行分析之前,首先应对收集到的数据进行数据清洗和质量控制,常用方法包括正态检验、T检验、卡方检验、批次检验。对预处理后的核糖核酸序列(RNA sequencing, RNA-Seq)数据,一般会根据数据的特征进行差异分析,常用方法有NOISeq、DESeq2、Limma、EdgeR等,各个方法的适用范围见表 1。
表 1 差异分析方法总结Table 1. Summary of difference analysis methods差异分析包 适用范围 NOISeq 可用于比较2个或多个条件下基因表达差异
适用于小样本的RNA测序数据DESeq2 可用于比较2组数据中的基因表达差异
适用于小样本、高度异变的数据差异分析
可用于评估药物处理对基因表达的影响Limma 适用于大规模样本量数据的差异分析
可读取数据和对数据进行预处理(如背景矫正、组内或组间标准化等)
可以对芯片和RNA-Seq数据进行差异分析,其线性模型和差异函数可以应用于任何基因表达定量技术EdgeR 可对RNA-Seq或ChIP-Seq等数据进行差异分析,也可对任何从基因组特征上产生的read count进行分析
既可用于多组实验的统计分析,也可使用广义线性模型方法来对多因子实验数据进行统计分析
不仅可以应用于基因水平,也可应用于外显子、转录组水平的差异分析2.2 基于基因组数据的乳腺癌分子预测
乳腺癌存在高度的异质性[26-27],即使对组织学类型、肿瘤淋巴结转移(tumor node metastasis,TNM)分期相同的乳腺癌患者采取相同的治疗方案,患者对治疗的反应和预后仍然有较大差异。因此,快速了解乳腺癌患者的肿瘤的良性/恶性情况,对个体化治疗的选择,如化疗、内分泌治疗和乳腺癌人表皮生长因子受体2(human epidermal growth factor receptor 2, HER2)靶向治疗,具有重要的指导价值。
由于基因测序价格昂贵且操作复杂,很多数据集都存在数据不均衡现象。为解决这个问题,Assegie等[28]基于从Kaggle上收集到的569例良性/恶性乳腺癌数据(其中良性样本占62.7%,恶性样本占37.3%),对比了自适应提升算法和决策树在进行良性/恶性预测时的性能,实验结果显示Adboost在亚型预测方面取得了优于决策树的性能。此外,为解决样本不均衡的问题,Naji等[29]对比了支持向量机(support vector machine,SVM)、随机森林(random forest, RF)、逻辑回归(logistic regression, LR)、决策树等有监督机器学习算法后发现SVM算法在维斯康星乳腺癌数据集(Wisconsin breast cancer dataset, WBCD)上取得了最优的预测效果。在WBCD上进行乳腺癌良性/恶性肿瘤分类的典型机器学习算法,包括SVM、LR、多层感知机(multilayer perceptron, MLP)、K最近邻(K-nearest neighbor, KNN)、RF、极度随机树(extremely randomized trees, Extra-Trees)、反向传播神经网络(backpropagation neural network, BPNN)、主成分分析(principal component analysis, PCA)、人工神经网络(artificial neural network, ANN)、深度置信网络(deep belief networks, DBN)、一维卷积神经网络(one-dimensional convolutional neural network, 1D-CNN),评价指标主要采用准确率(accuracy, ACC)、灵敏度(sensitivity, SE)、特异性(specificity, SP)、精确度(precision, PR)、召回率(recall, RE),如表 2所示。
表 2 乳腺癌良性/恶性预测方法概述Table 2. Overview of benign/malignant prediction methods for breast cancer方法 分类方法 文献 实验结果 传统机器学习 SVM Amrane等[30] ACC为0.962 SVM、LR、MLP Assiri等[31] ACC最大值为0.983 KNN Kumari等[32] ACC为0.993 SVM Asri等[33] ACC为0.971 3 RF、Extra-Trees Ghiasi等[34] ACC为1, SE为1, SP为1 深度学习 BPNN Nahato等[35] ACC为0.986 PCA、ANN Sahu等[36] ACC为0.97, SE为0.95, SP为0.98 ANN Alshayeji等[37] ACC为0.995, SE为0.996, SP为0.995 1D-CNN Asif等[38] ACC为0.983, PR为1, RE为0.953 MLP Agarap等[39] ACC为0.990 DBN、BPNN Abdel-Zaher等[40] ACC为0.997 鉴于临床上不同的乳腺癌患者具有不同的临床特征,Perou等[41]从基因表达水平上将乳腺癌定义为4种不同的固有亚型:Luminal A型、Luminal B型、HER2阳性型、三阴性型。因此,为实现乳腺癌的精确诊断和治疗,研究人员将机器学习应用于乳腺癌亚型预测研究中,并取得了较好的成绩。
PAM50是目前采用最广泛的乳腺癌亚型分类标准,但其易受到参考队列样本组成的影响。为提高PAM50分类的稳健性,Cascianelli等[42]提出了一种名为类内均值平均(average of within-class averages, AWCA)的策略,实验证明该策略具有超过90%的一致性和预测能力。许多基于深度学习的网络在训练和验证中都遇到了参数不足的情况,即参数的多种组合实现了相似的性能,当测试分布与训练分布不同时,某些参数组合可能表现不佳,因此,Anderson等[43]借鉴了Bui等[44]对标签传播和神经图模型的研究,提出了将先验知识嵌入机器学习系统的方法。该方法将先验知识嵌入到损失函数中,减少了深度学习架构上的预测变量的可变性,并增加了预测变量的一致性。
为进一步对组织学、临床学和分子特征进行综合诊断评分,促进基础癌症研究和精确的医学治疗,Binder等[45]提出了一个可解释的机器学习方法,该方法可以在组织学图像中稳健地检测癌细胞和肿瘤浸润淋巴细胞,并提供精确的热图对分类结果进行解释。其次,分子特征(包括DNA甲基化、基因表达、CNV、体细胞突变和蛋白质)均可从组织学中预测。该模型分子预测的平均准确率高达78%,患者亚组的准确率可达到95%以上。
另外,由于生物医学数据集往往是高维的,很多乳腺癌亚型分类算法的计算能力会受到限制,分类器也会受到不相关因素的影响,从而导致子类型模糊和重叠。为解决这个问题,Chen等[46]提出了一种深度学习框架DeepType,该方法在执行过程中联合了监督分类、无监督的聚类和维度降低,以学习具有集群结构的癌症相关数据表示。实验中将DeepType应用于METABRIC乳腺癌数据集,与现有方法相比它不仅取得了良好的分类性能,而且可以在使用更少基因的同时更好地识别出亚型。
以上研究表明,基于机器学习的分类算法可以深度挖掘乳腺癌基因序列数据中的隐藏特征,减少人为主观因素对乳腺癌影像分类的影响,实现对乳腺癌基因序列的自动化分型。由此可见,机器学习、大数据技术在乳腺癌分子分型研究、风险预测等领域的应用,促进了乳腺癌临床诊断的进步。乳腺癌的基因检测仍是侵入式的,而影像技术作为一种优良的非侵入式诊断方法,将在乳腺癌的精确诊断中发挥重要作用。
3. 乳腺癌影像组学研究
3.1 乳腺癌医学成像技术
目前,临床上用于乳腺癌检查的医学成像包括:乳腺X线摄影、DCE-MRI、超声成像、PET、CT等。由于每种方法的成像原理不同,每种检测工具都有其侧重。X线摄影常用于对患者进行初步检查,便于发现较明显病变的组织和结构且具有检查效率高、价廉等优点,但该方法一般只能提供组织重叠的二维平面影像,并且会出现病变区域显示不清或不能显示的情况;DCE-MRI能够进行多序列、多方向成像且能够清晰地显示软组织和解剖结构;超声成像方法可以对病灶区域进行实时多方向动态成像,并且由于价廉、简便、迅速、无创、无辐射、准确及可重复扫描等优点被广泛地应用到临床诊断中,但不适合含气脏器(如肺、消化道及骨骼)的检查;PET成像方法主要用于对高危人群的肿瘤筛查,该方法可以寻找转移瘤的原发部位,但具有一定假阴性病变且有一定的辐射;CT方法检查方便、迅速、密度分辨率高,可以提供没有组织重叠的横断面图像,并可进行不同平面的重建,但是,CT检查有一定辐射且对软组织肿瘤的诊断效能受衰减值的影响,导致医生可能无法鉴别肿瘤。
3.2 乳腺癌影像分割方法
影像分割是乳腺癌影像组学方法研究过程中的关键步骤。通过影像分割可以快速地识别乳腺癌影像中的病变区域,有助于提高后续诊断的准确率。
乳腺影像存在分辨率低、乳腺结构与病变位置易出现影像重叠、医学成像质量较差等问题,因此,对乳腺病变区域精确分割存在一定的难度。根据是否需要人机交互,可将医学成像分割方法分为3种:人工分割[47-48]、半自动分割、自动化分割[49-51]。目前,绝大多数影像组学研究仍然以手动分割为标准,然而手动分割需要放射科医生花费大量的时间和精力。国内外研究学者对乳腺病灶的半自动分割和自动化分割主要基于活动轮廓模型(active contour model, ACM)和深度学习的图像分割理论。本文对用于乳腺癌影像分割的方法进行了汇总,汇总结果见表 3。研究图像类型主要包括CT、PET、X线摄影、MRI等,研究方法主要包括U-Net、nnU-Net、融合全局和局部信息的水平集图像分割(global and local combined C-V, GLCCV)方法、马尔可夫随机场(Markov random fields, MRF)等,评价指标主要采用曲线下面积(area under curve, AUC)、戴斯相似性系数(Dice similarity coefficient, DICE)、SE、豪斯多夫距离(Hausdorff distance, HD)、交并比(intersection over union, IOU)、ACC、真阳性率(true positive ratio, TPR)、假阳性概率(false positive ratio, FPR)、假阴性率(false negative ratio, FNR)、相似率(similarity ratio, SIR)、Hausdorff误差(Hausdorff error, HE)等。
表 3 乳腺癌病变分割概述Table 3. Overview of breast cancer lesion segmentation算法 分割方法 文献 数据集 图像类型 实验结果 基于深度学习的分割算法 U-Net Benjelloun等[52] 86个DCE-MRI影像和43位患者的5 452个乳腺局部组织切片 DCE-MRI IoU为0.761 4 U-Net Huo等[53] 复旦大学附属肿瘤医院的100份乳腺DCE-MR扫描结果 DCE-MR DICE为0.968±0.017 RF+U-Net Cabrera等[54] 1 959个肿瘤向量和26 184个非肿瘤向量 PET/CT SE为0.952±0.017 Hybrid CNN/C-Tree Cabrera等[55] 52名患者的240个淋巴结病理影像 PET/CT 基于区域的分割获得的SE为0.933±0.075 DeepLab、Mask R-CNN Ahmed等[56] MIAS、CBIS-DDSM X线摄影 R-CNN模型在分割任务中获得的平均AUC为0.80,DeepLab模型在分割任务中获得的平均AUC为0.75 生成对抗+卷积神经网络 Singh等[57] DDSM+INbreast 乳房X线摄影 DICE为0.94IoU为0.87 基于ACM的分割算法 结合MRF和DCE-MRI时域特征的混合ACM 周皓阳等[58] 20张乳腺DCE-MRI图像 DCE-MRI DICE为0.84,HD为2.78 ACM Keatmanee等[59] 泰国法政大学医院收集的90张图片 超声波图像 ACC为0.889 图切割ACM Daoud等[60] 约旦大学医院收集的86例良性和74例恶性病例图像 超声波图像 TPR为0.960
FPR为0.079 9
FNR为0.039 6
SIR为0.914 1
HE为0.116 6
平均绝对误差(mean absolute error, MAE)为0.036 5GLCCV 张旭梅等[61] 医学数字成像和通信(digital imaging and communications in medicine, DICOM)格式的临床乳腺MRI 乳腺MRI图像 平均误差(mean error, ME)为2.293 1 基于水平集的多尺度乳腺肿块分割方法 虞红伟等[62] 89例肿块病灶图像 乳腺X线图像 误分率为0.236 1 3D病灶分割方法 Kuo等[63] 33名患者的38个肿块(25个恶性、13个良性) CT图像 DICE最大值为0.81 基于背景分布的ACM Liu等[64] 46个病变包含29个良性病变和17个恶性病变 DCE-MRI 重叠率为79.55%±12.60% 基于深度学习的分割方法(如卷积神经网络和全卷积神经网络)也被应用在乳腺癌影像的病灶分割中。Kallenberg等[65]把无监督深度学习应用到乳腺癌病灶分割。Rouhi等[66]提出了2种基于神经网络的分割方法:一是通过训练人工神经网络确定自动区域的增长阈值达到分割乳腺癌病灶的目的;二是通过细胞式神经网络执行分割,网络的参数由遗传算法得出。Ashraf等[67]使用多通道MRF对动态观测模型的乳腺DCE-MRI数据进行自动分割。
为实现乳腺癌病灶区域的自动分割,Huo等[53]采用基于深度学习细分框架的nnU-Net实现了对乳腺和纤维腺组织的DCE-MR影像的高效率、高精度分割。Yin等[68]将直方图与逆高斯分布梯度相结合,并扩展了Stein无偏风险估计,形成了无监督的深度神经网络高斯分类器,从含有噪声的乳腺MRI影像中自动分割了病灶区域与正常组织。通过深度学习技术实现癌变区域的自动分割法能更好地排除人为因素的影响,但目前的分割准确率还不能满足临床应用要求,因此,难以在临床上得到广泛的应用。
目前,乳腺癌放射组学研究仍处于早期阶段,乳腺癌影像组学研究仍是未来的一个重要研究方向。
3.3 乳腺癌影像特征提取
通过乳腺癌影像癌变区域的语义分割模型对影像进行切割后,可以得到整体病灶区域和非病灶区域,之后需要对这些区域进行影像特征的提取。根据图像生物标志物标准化倡议(image biomarker standardization initiative, IBSI)提出的标准,图像特征大致分为4类[69]:1) 一阶灰度统计特征。该特征指基于描述图像中的体素强度分布的一阶直方图计算出的基本特征。常用的特征有能量、峰度、偏度等。2) 基于形态的特征。该特征用于描述肿瘤的几何形状,常用的特征有体积、表面积、球形度、直径和平面度等。3) 纹理特征。该特征用于描述像素之间的相关性,包括灰度共生矩阵、灰度区域大小矩阵、灰度依赖矩阵、邻域灰度差分矩阵、灰度游程矩阵等。4) 基于变换的特征。该特征指在原图像上施加变换,如Log变换或小波变换。此外,不同的研究团队所提取的影像特征也不同,本文总结了Zhu等[70]所划分的6类DCE-MRI影像特征,如表 4所示。
表 4 DCE-MRI影像特征Table 4. Image characteristics of DCE-MRI类别 名称 表型大小 病灶体积、有效直径、表面积、最大线性尺寸 表型形状 球度、不规则性、比表面积 表型形态 边缘锐度、边缘锐度的差异、径向梯度直方图的方差 增强纹理表型 角二阶距、相关性、熵、逆差分矩等 动力学曲线评估 最大增强值、达峰时间、对比度增强的吸收速度、曲线形状指数、首次对比度增强后的时间点等 增强方差动力学 增强扫描最大方差 4. 特征选择与模型构建
4.1 影像特征的选择
将通过乳腺癌影像癌变区域的语义分割和对病灶区域进行影像特征提取得到的大量影像特征用于模型训练,可能会发生“维度灾难”而造成模型的过拟合[71]。因此,需要使用特征提取方法从大量的特征中提取出能够获得最佳性能表征的特征集。特征的好坏并没有标准的定义,要视具体的问题或应用而定。良好的特征通常具备可区分性、可靠性、独立性、数量少等特点。
常用的特征提取方法主要分为3类[72]:1) 过滤式选择。该方法是指不考虑模型算法而根据特定的性能度量对特征进行排序,然后按照指定阈值选择特征。优点是计算速度快、可扩展且独立于具体的算法。常用方法有Lasso Cox回归模型[73]、岭回归等。缺点是缺乏与分类器的交互作用,会造成分类准确率较低。2) 包裹式选择。该方法是指通过机器学习算法评估特征子集,通过搜索得到所有可能的特征子集,之后对每个子集进行评估,因此,通过该方法找到的特征子集的分类性能通常更好。但包裹式选择方法所得到的特征集通用性不强,此外,当学习算法的计算复杂度很高或训练数据为大规模数据集时,算法的执行时间会很长。常用的特征筛选方法有枚举搜索、递归特征消除、顺序向前选择算法、顺序后向生成和遗传算法[74]等。3) 嵌入式选择。该方法是指在模型训练期间进行特征选择,结合了过滤式和包裹式选择方法的优点,既考虑到包裹式选择方法中特征与模型的交互作用,又考虑到过滤式选择方法的运行速度和准确率。常用的方法有正则化、RF[75]等。
4.2 模型的构建
模型的建立是乳腺癌影像基因组学研究的最终目的。通过乳腺癌基因组学的研究,挖掘乳腺癌以基因为代表的生物大分子与影像特征之间的联系,通过影像特征反映基因活动,辅助医生进行乳腺癌的诊断和治疗。在影像基因组学建模中,常用的机器学习方法有多元LR模型[76]、RF[77-78]、SVM[79]、聚类分析[80]、神经网络[81-83]等。本文详细描述了机器学习技术在乳腺癌影像基因组学模型构造中的应用现状,如表 5所示。
表 5 乳腺癌影像基因组学模型概述Table 5. Overview of breast cancer imaging genomics models文献 数据 方法 实验结果 Yamamoto等[84] 基因表达值、MRI影像特征 斯皮尔曼等级相关系数 21个影像特征与71%的基因存在全基因组范围内的关联(p<0.05);12个影像特征和乳腺癌基因集存在显著关联(FPR小于0.25),11个影像特征与预后基因集存在关联(FPR小于0.25) Liu等[85] MRI影像特征、临床病理特征 LR模型 AUC为0.869 Wang等[86] 基因组信息、病理图像数据 CNN模型 基于放大倍数为40、20、10、5的图像获得的AUC分别为0.766、0.763、0.750、0.551 Mazurowski等[87] 分子亚型、MRI影像特征 多元LR分析 Luminal B型乳腺癌与动态造影剂增强特征存在关联(p=0.001 5) Liu等[88] SNP、影像特征 关联分析 有11组SNP特征和影像特征对与乳腺癌发生风险显著相关,其中,6组与乳腺癌风险增加相关,5组与乳腺癌风险降低相关 Sun等[89] 乳腺超声、分子亚型 CNN模型 CNN模型获得了较好的预测性能;结合瘤内和瘤周区域模型获得了更好的预测性能 Liu等[90] 基因模态数据、图像模态数据 基于多模态数据的混合深度学习模型 AUC为0.9427 Lin等[91] MRI影像特征、遗传信息 假设检验+最小绝对收缩和选择算子(least absolute shrinkage and selection operator, LASSO)算法 预测细胞周期获得的AUC为0.933; 预测Myc获得的AUC为0.926;预测PI3K获得的AUC为0.956; 预测RTK/RAS获得的AUC为0.940;预测p53获得的AUC为0.886 为探究影像基因组学对疗效及预后的预测价值,Yamamoto等[84]从353例乳腺癌患者的基因组内获得高差异性表达基因,并采用人工方法评估了26个MRI影像特征,利用斯皮尔曼等级相关系数建立基因与影像特征之间的关联,然后进行了基因集富集分析。实验结果显示:21个影像特征与71%的基因存在全基因组范围内的关联(p<0.05);12个影像特征和乳腺癌基因集存在显著关联(FPR小于0.25);11个影像特征与预后基因集存在关联(FPR小于0.25)。Liu等[85]对163个乳腺癌患者(55个前哨淋巴转移、108个前哨淋巴未转移)使用DCE-MRI对肿瘤内和肿瘤周围组织进行了成像,实验中采用LR将放射组学特征分别结合或不结合原发肿瘤的临床病理特征,成功实现了无创地预测乳腺癌的前哨淋巴结转移状态(AUC为0.869)。Wang等[86]基于病理图像数据和分子组学数据训练了CNN模型用于预测乳腺癌基因突变。实验结果揭示了病理图像与基因突变之间的相关性,证明了深度CNN能够协助病理学家检测基因突变。为研究影像特征与分子亚型之间的联系,Mazurowski等[87]从48例患者中提取了23个MRI影像特征,并通过基因表达分析获得4个乳腺癌分子亚型。对4种乳腺癌分子亚型和影像特征进行了多元LR分析,并分析了乳腺影像特征和分子分型之间的联系。实验结果表明,Luminal B型乳腺癌与动态造影剂增强特征存在关联(p=0.001 5)。为建立乳腺癌风险的评估模型,Liu等[88]首次进行了乳腺癌SNP和影像特征的关联分析,使用55个SNP和49个乳腺X线摄影影像特征构造了关联模型。实验结果显示,有11组SNP和影像特征对与乳腺癌发生风险显著相关,其中,6组与乳腺癌风险增加相关,5组与乳腺癌风险降低相关。
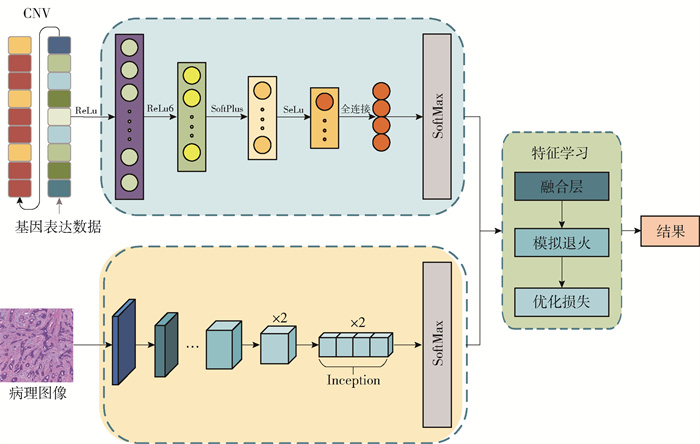
目前,很多深度学习算法也被应用于乳腺癌影像基因组学模型的构建。Sun等[89]利用乳腺超声预测腋窝淋巴结(axillary lymph node, ALN)转移状态。一方面,基于瘤内、瘤周以及瘤内和瘤周联合区域分别使用DenseNet构造了3个CNN模型,在训练/测试队列中获得的AUC分别为0.937/0.748、0.944/0.775、0.957/0.912。使用RF构造了3个放射组学模型,在训练/测试队列中获得的AUC分别为0.913/0.693、0.920/0.724、0.940/0.886。另一方面,将乳腺癌分子亚型与以上6个模型结合,构造了6个基于分子亚型的模型,在训练/测试队列中获得的AUC分别为0.931/0.794、0.951/0.813、0.962/0.933。实验结果表明:CNN模型相对于放射组学模型获得了较好的预测性能;相对于CNN和放射组学模型,结合瘤内和瘤周区域获得了更好的预测性能。大多数传统的深度学习模型使用的是单模态数据,只能提取一些特征,因此,无法在患者特征和乳腺癌亚型之间建立稳定的关系。Liu等[90]利用公开的TCGA-BRCA数据集提出了一种基于多模态数据的混合深度学习模型(见图 1)。该模型将乳腺癌患者的基因模态数据与图像模态数据相结合,构建多模态融合框架。根据不同的形式和状态,分别构建了特征提取网络,然后基于加权线性聚合的思想融合2个特征网络的输出。最后,将融合特征用于预测乳腺癌分子亚型。实验结果显示,相对于传统的深度学习模型,该模型在预测乳腺癌亚型方面具有更高的准确性和效率,获得的平均AUC值为0.942 7,比以前的平均水平高约7.45%。由此可知,将神经网络应用于乳腺癌影像基因组学取得了较好的实验结果,并且神经网络在影像特征提取方面表现出优异的性能,但是,深度学习模型存在不可解释性且训练过程需要大量图像数据的问题,这是将神经网络应用于乳腺癌影像基因组学所面临的挑战之一。因此,如何更好地将深度学习应用于乳腺癌影像基因组学还需进一步研究。
5. 影像基因组学分析工具
影像基因组学包括影像组学分析、基因组学分析以及影像基因组学模型构建,由于该学科涉及医学和工科的知识且分析步骤复杂,因此,对研究人员提出了更高的要求。然而,科学技术的快速发展,使得研究人员可以借助一些分析工具达到研究的目的。目前,基于乳腺癌影像基因组学的研究所使用到的分析工具可以分为3类。
1) 分析数据库。为探究癌症的发病机制,大规模的癌症基因组计划正在从多技术平台产生更多的癌症基因组数据,使得多组学大规模数据的整合与分析变得越来越具有挑战性,对于没有计算机背景知识的研究人员来说更是如此。因此,为降低研究的复杂性,很多大型公开数据库都提供了数据的可视化分析功能。常用的乳腺癌基因组学分析数据库如表 6所示,包括癌症基因组图谱(the cancer genome atlas, TCGA)数据库、高通量基因表达(gene expression omnibus, GEO)数据库、cBioPortal数据库等。其中TCGA数据库对20 000多种原发性癌症进行了分子表征,并匹配了33种癌症类型的正常样本,TCGA产生了超过2.5 PB的基因组、表观基因组、转录组和蛋白质组学数据,是癌症研究者很重要的数据来源。GEO数据库为研究人员提供了一个广泛的基因表达数据集合,涵盖了多个物种和研究领域,包括基础生物学、医学研究和生物信息学等。该数据库用于存档和免费分发研究人员提交的微阵列、下一代测序和其他形式的高通量功能基因组学数据。cBioPortal数据库整合了126种肿瘤基因组数据,用户可以可视化地进行生物通路探索、生存分析、基因间的相互独特性分析,另外,用户可选择性地进行数据下载。GEPIA数据库包含了最全面的TCGA测序数据,能够可视化肿瘤与癌旁组织的基因表达量,可以实现单基因分析、癌种分析、多基因分析。UCSC Xena是一个癌症基因组学数据分析平台,支持对癌症样本的多种组学数据进行可视化分析。基因表达数据的分析是影像基因组学中的关键步骤,上述公开数据库所提供的分析工具可以帮助研究人员快速地了解基因表达特征以及基因间的相互关系,其中cBioPortal、GEPIA和Fire Browse数据库都是基于TCGA数据库所开发的分析平台,具有图形化界面且操作简单,适合初入该领域的研究人员,其缺点是数据库内仅提供肿瘤数据。Kaplan Meier Plotter、cBioPortal数据库都可对患者进行生存分析,但都不能调整生存曲线的配色。
表 6 乳腺癌影像基因组学分析数据库概述Table 6. Overview of breast cancer imaging genomics analysis database数据库 功能描述 网址 TCGA 提供多种癌症的基因组测序数据下载,包括表观基因组学、转录组学、蛋白质组学等 https://portal.gdc.cancer.gov/ GEO 提供基础生物学、医学和生物信息学等多个领域的微阵列、高通量功能基因组学等数据下载 cBioPortal 生物通路探索、生存分析、基因间的相互独特性分析;数据下载 https://www.cbioportal.org/ 基因表达谱交互分析(gene expression profiling interactive analysis, GEPIA) 单基因分析、癌种分析、多基因分析 http://gepia.cancer-pku.cn/ Fire Browse 基因表达分析、突变分析 http://firebrowse.org/ Kaplan Meier Plotter 生存分析 http://kmplot.com/analysis/ UCSC Xena 多种组学数据的可视化分析 https://xenabrowser.net/ StarBase miRNA-mRNA、RNA结合蛋白(RNA-binding proteins, RBP)-RNA、RNA-RNA相互作用 http://starbase.sysu.edu.cn/index.php 京都基因与基因组百科全书(Kyoto Encyclopedia of Genes and Genomes, KEGG) 可视化代谢途径以及各途径之间的关系 https://www.genome.jp/kegg/ Oncomine 计算基因表达特征和聚类基因集,可以进行生物学功能分析 https://www.oncomine.com/ 癌症体细胞突变目录(catalogue of somatic mutations in cancer, COSMIC) 蛋白结构和功能的变化以及对药物的影响;数据下载 https://cancer.sanger.ac.uk/cosmic/ 2) 分析软件。SPSS[92]是一款数据分析软件,可进行多元统计分析、统计相关模型构建、时间序列建模等。Tableau软件可以帮助研究人员快速分析并可视化数据。另外,常用的ROI分割工具有MIM(https://www.mimsoftware.com)、ITK-SNAP(http://www.itksnap.org)、3DSlicer(http://www.slicer.org)和ImageJ(https://imagej.nih.gov/ij/)等半自动和全自动分割软件。常用的影像特征提取软件有:IBEX[93]、MaZda[94]、CERR、PORTS 3D等。模型构建常用的软件有:SPSS Modeler[92]、B11[95]、Weka[96]、R语言等。其中IBEX、CERR和MaZda软件开源且具有图形化界面,缺点是特征的类型固定,可扩展性差。Weka和SPSS Modeler软件是模型构建时常采用的软件,二者功能强大且具有图形界面,适合大多数研究人员,R语言较适合具有编程能力的研究人员[97]。
3) 编码语言。基因组学分析时常用的编码语言有R语言,其中常用到的软件包有ggplot2、WGCNA、GSVA、Limma、Caret等[98-99]。Python是一种面向对象的语言,语法直观易懂,并为用户提供了许多深度学习库,如TensorFlow、Caffe、Torch等[100-101]。MATLAB是一款商用软件,可以进行矩阵运算、实现算法、创建用户界面、连接其他编程语言的程序等[102-103]。编码语言是影像基因组学进行分析的常用工具,其中R语言和Python均是免费的软件,相对于MATLAB,二者均具有简单、易学、严谨等优点,但MATLAB的专业性很强的工具箱仍是R语言和Python不能代替的。
由于影像基因组学分析是一种高通量的数据分析方法,其对数据预处理和标准化,特征的提取和筛选以及模型的构建和预测都提出了很高的要求。目前,存在很多基于影像基因组学的研究工具,但研究过程中还须结合数据特征选择合适的研究工具,实现影像基因组学数据的深度挖掘。
6. 总结与展望
1) 随着机器学习与影像基因组学的发展,利用机器学习算法挖掘乳腺癌基因组学数据和影像组学数据的潜在信息,可以促进乳腺癌医学诊断与治疗的进步,提高乳腺癌临床诊断的准确率和效率,减少医生的工作量。影像基因组学是将基因组学和影像组学相关联的一个新兴领域,虽然机器学习方法在该领域的应用在一定程度上解决了一些问题,但组学相关联仍是一个新兴领域。目前,机器学习方法在乳腺癌影像基因组学研究中仍存在一些局限性,主要如下:
① 由于乳腺癌癌变区域具有复杂性且缺少简单的线性特征,当面对复杂结构的乳腺癌影像数据时,自动化分割技术的分割结果往往不能满足临床应用的要求,未来工作中还需进一步研究。
② 基因检测价格昂贵、操作复杂且基因表达和信号通路极其复杂,研究人员需要大量的生物学知识,这限制了乳腺癌影像基因组学的研究。
③ 现有的机器学习方法往往需要大规模地标注数据,但高质量医学图像很难获取且人工标注成本较高。因此,在未来的工作中急需开展无监督或弱监督问题的研究。
④ 将深度学习应用到乳腺癌临床诊断的前提是所构建的模型具有足够的可信度和可解释性,而简单的回顾性研究不具有足够的可信度,难以满足临床要求。因此,未来有必要开展可解释性模型在乳腺癌影像基因组学问题上的研究。
2) 目前,乳腺癌影像基因组学仍是一个新兴的研究领域,但因其可建立乳腺癌基因组学和乳腺癌影像组学的关联模型,在可预见的未来仍有望提高乳腺癌临床诊断、预后评估和治疗的准确率,实现乳腺癌的精准治疗。机器学习和大数据技术的应用在促进乳腺癌影像基因组学进步的同时也带来了一些局限性,因此,在未来工作中还须对其进行深入研究。
-
表 1 差异分析方法总结
Table 1 Summary of difference analysis methods
差异分析包 适用范围 NOISeq 可用于比较2个或多个条件下基因表达差异
适用于小样本的RNA测序数据DESeq2 可用于比较2组数据中的基因表达差异
适用于小样本、高度异变的数据差异分析
可用于评估药物处理对基因表达的影响Limma 适用于大规模样本量数据的差异分析
可读取数据和对数据进行预处理(如背景矫正、组内或组间标准化等)
可以对芯片和RNA-Seq数据进行差异分析,其线性模型和差异函数可以应用于任何基因表达定量技术EdgeR 可对RNA-Seq或ChIP-Seq等数据进行差异分析,也可对任何从基因组特征上产生的read count进行分析
既可用于多组实验的统计分析,也可使用广义线性模型方法来对多因子实验数据进行统计分析
不仅可以应用于基因水平,也可应用于外显子、转录组水平的差异分析表 2 乳腺癌良性/恶性预测方法概述
Table 2 Overview of benign/malignant prediction methods for breast cancer
方法 分类方法 文献 实验结果 传统机器学习 SVM Amrane等[30] ACC为0.962 SVM、LR、MLP Assiri等[31] ACC最大值为0.983 KNN Kumari等[32] ACC为0.993 SVM Asri等[33] ACC为0.971 3 RF、Extra-Trees Ghiasi等[34] ACC为1, SE为1, SP为1 深度学习 BPNN Nahato等[35] ACC为0.986 PCA、ANN Sahu等[36] ACC为0.97, SE为0.95, SP为0.98 ANN Alshayeji等[37] ACC为0.995, SE为0.996, SP为0.995 1D-CNN Asif等[38] ACC为0.983, PR为1, RE为0.953 MLP Agarap等[39] ACC为0.990 DBN、BPNN Abdel-Zaher等[40] ACC为0.997 表 3 乳腺癌病变分割概述
Table 3 Overview of breast cancer lesion segmentation
算法 分割方法 文献 数据集 图像类型 实验结果 基于深度学习的分割算法 U-Net Benjelloun等[52] 86个DCE-MRI影像和43位患者的5 452个乳腺局部组织切片 DCE-MRI IoU为0.761 4 U-Net Huo等[53] 复旦大学附属肿瘤医院的100份乳腺DCE-MR扫描结果 DCE-MR DICE为0.968±0.017 RF+U-Net Cabrera等[54] 1 959个肿瘤向量和26 184个非肿瘤向量 PET/CT SE为0.952±0.017 Hybrid CNN/C-Tree Cabrera等[55] 52名患者的240个淋巴结病理影像 PET/CT 基于区域的分割获得的SE为0.933±0.075 DeepLab、Mask R-CNN Ahmed等[56] MIAS、CBIS-DDSM X线摄影 R-CNN模型在分割任务中获得的平均AUC为0.80,DeepLab模型在分割任务中获得的平均AUC为0.75 生成对抗+卷积神经网络 Singh等[57] DDSM+INbreast 乳房X线摄影 DICE为0.94IoU为0.87 基于ACM的分割算法 结合MRF和DCE-MRI时域特征的混合ACM 周皓阳等[58] 20张乳腺DCE-MRI图像 DCE-MRI DICE为0.84,HD为2.78 ACM Keatmanee等[59] 泰国法政大学医院收集的90张图片 超声波图像 ACC为0.889 图切割ACM Daoud等[60] 约旦大学医院收集的86例良性和74例恶性病例图像 超声波图像 TPR为0.960
FPR为0.079 9
FNR为0.039 6
SIR为0.914 1
HE为0.116 6
平均绝对误差(mean absolute error, MAE)为0.036 5GLCCV 张旭梅等[61] 医学数字成像和通信(digital imaging and communications in medicine, DICOM)格式的临床乳腺MRI 乳腺MRI图像 平均误差(mean error, ME)为2.293 1 基于水平集的多尺度乳腺肿块分割方法 虞红伟等[62] 89例肿块病灶图像 乳腺X线图像 误分率为0.236 1 3D病灶分割方法 Kuo等[63] 33名患者的38个肿块(25个恶性、13个良性) CT图像 DICE最大值为0.81 基于背景分布的ACM Liu等[64] 46个病变包含29个良性病变和17个恶性病变 DCE-MRI 重叠率为79.55%±12.60% 表 4 DCE-MRI影像特征
Table 4 Image characteristics of DCE-MRI
类别 名称 表型大小 病灶体积、有效直径、表面积、最大线性尺寸 表型形状 球度、不规则性、比表面积 表型形态 边缘锐度、边缘锐度的差异、径向梯度直方图的方差 增强纹理表型 角二阶距、相关性、熵、逆差分矩等 动力学曲线评估 最大增强值、达峰时间、对比度增强的吸收速度、曲线形状指数、首次对比度增强后的时间点等 增强方差动力学 增强扫描最大方差 表 5 乳腺癌影像基因组学模型概述
Table 5 Overview of breast cancer imaging genomics models
文献 数据 方法 实验结果 Yamamoto等[84] 基因表达值、MRI影像特征 斯皮尔曼等级相关系数 21个影像特征与71%的基因存在全基因组范围内的关联(p<0.05);12个影像特征和乳腺癌基因集存在显著关联(FPR小于0.25),11个影像特征与预后基因集存在关联(FPR小于0.25) Liu等[85] MRI影像特征、临床病理特征 LR模型 AUC为0.869 Wang等[86] 基因组信息、病理图像数据 CNN模型 基于放大倍数为40、20、10、5的图像获得的AUC分别为0.766、0.763、0.750、0.551 Mazurowski等[87] 分子亚型、MRI影像特征 多元LR分析 Luminal B型乳腺癌与动态造影剂增强特征存在关联(p=0.001 5) Liu等[88] SNP、影像特征 关联分析 有11组SNP特征和影像特征对与乳腺癌发生风险显著相关,其中,6组与乳腺癌风险增加相关,5组与乳腺癌风险降低相关 Sun等[89] 乳腺超声、分子亚型 CNN模型 CNN模型获得了较好的预测性能;结合瘤内和瘤周区域模型获得了更好的预测性能 Liu等[90] 基因模态数据、图像模态数据 基于多模态数据的混合深度学习模型 AUC为0.9427 Lin等[91] MRI影像特征、遗传信息 假设检验+最小绝对收缩和选择算子(least absolute shrinkage and selection operator, LASSO)算法 预测细胞周期获得的AUC为0.933; 预测Myc获得的AUC为0.926;预测PI3K获得的AUC为0.956; 预测RTK/RAS获得的AUC为0.940;预测p53获得的AUC为0.886 表 6 乳腺癌影像基因组学分析数据库概述
Table 6 Overview of breast cancer imaging genomics analysis database
数据库 功能描述 网址 TCGA 提供多种癌症的基因组测序数据下载,包括表观基因组学、转录组学、蛋白质组学等 https://portal.gdc.cancer.gov/ GEO 提供基础生物学、医学和生物信息学等多个领域的微阵列、高通量功能基因组学等数据下载 cBioPortal 生物通路探索、生存分析、基因间的相互独特性分析;数据下载 https://www.cbioportal.org/ 基因表达谱交互分析(gene expression profiling interactive analysis, GEPIA) 单基因分析、癌种分析、多基因分析 http://gepia.cancer-pku.cn/ Fire Browse 基因表达分析、突变分析 http://firebrowse.org/ Kaplan Meier Plotter 生存分析 http://kmplot.com/analysis/ UCSC Xena 多种组学数据的可视化分析 https://xenabrowser.net/ StarBase miRNA-mRNA、RNA结合蛋白(RNA-binding proteins, RBP)-RNA、RNA-RNA相互作用 http://starbase.sysu.edu.cn/index.php 京都基因与基因组百科全书(Kyoto Encyclopedia of Genes and Genomes, KEGG) 可视化代谢途径以及各途径之间的关系 https://www.genome.jp/kegg/ Oncomine 计算基因表达特征和聚类基因集,可以进行生物学功能分析 https://www.oncomine.com/ 癌症体细胞突变目录(catalogue of somatic mutations in cancer, COSMIC) 蛋白结构和功能的变化以及对药物的影响;数据下载 https://cancer.sanger.ac.uk/cosmic/ -
[1] BRAY F, LAVERSANNE M, WEIDERPASS E, et al. The ever-increasing importance of cancer as a leading cause of premature death worldwide[J]. Cancer, 2021, 127(16): 3029-3030. doi: 10.1002/cncr.33587
[2] SIEGEL R L, MILLER K D, FUCHS H E, et al. Cancer statistics, 2022[J]. CA: A Cancer Journal for Clinicians, 2022, 72(1): 7-33. doi: 10.3322/caac.21708
[3] XIA C F, DONG X S, LI H, et al. Cancer statistics in China and United States, 2022: profiles, trends, and determinants[J]. Chinese Medical Journal, 2022, 135(5): 584-590. doi: 10.1097/CM9.0000000000002108
[4] RUTMAN A M, KUO M D. Radiogenomics: creating a link between molecular diagnostics and diagnostic imaging[J]. European Journal of Radiology, 2009, 70(2): 232-241. doi: 10.1016/j.ejrad.2009.01.050
[5] NOUGARET S, MCCAGUE C, TIBERMACINE H, et al. Radiomics and radiogenomics in ovarian cancer: a literature review[J]. Abdominal Radiology, 2021, 46(6): 2308-2322. doi: 10.1007/s00261-020-02820-z
[6] LO GULLO R, DAIMIEL I, MORRIS E A, et al. Combining molecular and imaging metrics in cancer: radiogenomics[J]. Insights into Imaging, 2020, 11(1): 1. doi: 10.1186/s13244-019-0795-6
[7] WOODARD G A, RAY K M, JOE B N, et al. Qualitative radiogenomics: association between Oncotype DX test recurrence score and BI-RADS mammographic and breast MR imaging features[J]. Radiology, 2018, 286(1): 60-70. doi: 10.1148/radiol.2017162333
[8] GRIMM L J. Breast MRI radiogenomics: current status and research implications[J]. Journal of Magnetic Resonance Imaging, 2016, 43(6): 1269-1278. doi: 10.1002/jmri.25116
[9] HUANG Q W, ZHOU Y Z, TAO L M, et al. A Chan-Vese model based on the Markov chain for unsupervised medical image segmentation[J]. Tsinghua Science and Technology, 2021, 26(6): 833-844. doi: 10.26599/TST.2020.9010042
[10] 陆浥尘, 胡屹玲. 医学影像人工智能的研发应用现状与挑战[J]. 人工智能, 2021(3): 11-19. https://www.cnki.com.cn/Article/CJFDTOTAL-DKJS202103005.htm LU Y C, HU Y L. Current status and challenges of research and development and application of artificial intelligence in medical imaging[J]. Artificial Intelligence, 2021(3): 11-19. (in Chinese) https://www.cnki.com.cn/Article/CJFDTOTAL-DKJS202103005.htm
[11] WANG J, ZHU H D, WANG S H, et al. A review of deep learning on medical image analysis[J]. Mobile Networks and Applications, 2021, 26(1): 351-380. doi: 10.1007/s11036-020-01672-7
[12] SHEN D, WU G, SUK H I. Deep learning in medical image analysis[J]. Annual Review of Biomedical Engineering, 2017, 19: 221-248. doi: 10.1146/annurev-bioeng-071516-044442
[13] CRIMINISI A. Machine learning for medical images analysis[J]. Medical Image Analysis, 2016, 33: 91-93. doi: 10.1016/j.media.2016.06.002
[14] 周瑞泉, 纪洪辰, 刘荣. 智能医学影像识别研究现状与展望[J]. 第二军医大学学报, 2018, 39(8): 917-922. https://www.cnki.com.cn/Article/CJFDTOTAL-DEJD201808022.htm ZHOU R Q, JI H C, LIU R. Intelligent medical image recognition: progress and prospect[J]. Academic Journal of the Second Military Medical University, 2018, 39(8): 917-922. (in Chinese) https://www.cnki.com.cn/Article/CJFDTOTAL-DEJD201808022.htm
[15] SALA E, MEMA E, HIMOTO Y, et al. Unravelling tumour heterogeneity using next-generation imaging: radiomics, radiogenomics, and habitat imaging[J]. Clinical Radiology, 2017, 72(1): 3-10. doi: 10.1016/j.crad.2016.09.013
[16] 魏竹馨, 文玲, 王希明. 影像基因组学在乳腺癌中的研究现状与进展[J]. 国际医学放射学杂志, 2020, 43(6): 681-685, 692. https://www.cnki.com.cn/Article/CJFDTOTAL-GWLC202006014.htm WEI Z X, WEN L, WANG X M. Research status and progress of radiogenomics in breast cancer[J]. International Journal of Medical Radiology, 2020, 43(6): 681-685, 692. (in Chinese) https://www.cnki.com.cn/Article/CJFDTOTAL-GWLC202006014.htm
[17] BODALAL Z, TREBESCHI S, NGUYEN-KIM T D L, et al. Radiogenomics: bridging imaging and genomics[J]. Abdominal Radiology, 2019, 44(6): 1960-1984. doi: 10.1007/s00261-019-02028-w
[18] LAMBIN P, RIOS-VELAZQUEZ E, LEIJENAAR R, et al. Radiomics: extracting more information from medical images using advanced feature analysis[J]. European Journal of Cancer, 2012, 48(4): 441-446. doi: 10.1016/j.ejca.2011.11.036
[19] KUMAR V, GU Y H, BASU S, et al. Radiomics: the process and the challenges[J]. Magnetic Resonance Imaging, 2012, 30(9): 1234-1248. doi: 10.1016/j.mri.2012.06.010
[20] WANG T, GONG J, DUAN H H, et al. Correlation between CT based radiomics features and gene expression data in non-small cell lung cancer[J]. Journal of X-ray Science and Technology, 2019, 27(5): 773-803. doi: 10.3233/XST-190526
[21] XIA T, KUMAR A, FULHAM M, et al. Fused feature signatures to probe tumour radiogenomics relationships[J]. Scientific Reports, 2022, 12(1): 2173. doi: 10.1038/s41598-022-06085-y
[22] SUI D, GUO M, MA X X, et al. Imaging biomarkers and gene expression data correlation framework for lung cancer radiogenomics analysis based on deep learning[J]. IEEE Access, 2021, 9: 125247-125257. doi: 10.1109/ACCESS.2021.3071466
[23] 贾宇珊, 吴慧. 影像基因组学研究进展[J]. 磁共振成像, 2022, 13(3): 166-170. https://www.cnki.com.cn/Article/CJFDTOTAL-CGZC202203040.htm JIA Y S, WU H. Research advances in radiogenomics[J]. Chinese Journal of Magnetic Resonance Imaging, 2022, 13(3): 166-170. (in Chinese) https://www.cnki.com.cn/Article/CJFDTOTAL-CGZC202203040.htm
[24] COURT L E, FAVE X, MACKIN D, et al. Computational resources for radiomics[J]. Translational Cancer Research, 2016, 5(4): 340-348. doi: 10.21037/tcr.2016.06.17
[25] 明文龙, 袁少勋, 谢建明, 等. 乳腺癌影像基因组学研究进展[J]. 中国医学影像学杂志, 2018, 26(12): 952-956. doi: 10.3969/j.issn.1005-5185.2018.12.017 MING W L, YUAN S X, XIE J M, et al. Research progress in imaging genomics of breast cancer[J]. Chinese Journal of Medical Imaging, 2018, 26(12): 952-956. (in Chinese) doi: 10.3969/j.issn.1005-5185.2018.12.017
[26] KOBOLDT D D, FULTON R S, MCLELLAN M D, et al. Comprehensive molecular portraits of human breast tumours[J]. Nature, 2012, 490(7418): 61-70. doi: 10.1038/nature11412
[27] HOLM J, ERIKSSON L, PLONER A, et al. Assessment of breast cancer risk factors reveals subtype heterogeneity[J]. Cancer Research, 2017, 77(13): 3708-3717. doi: 10.1158/0008-5472.CAN-16-2574
[28] ASSEGIE T A, TULASI R L, KUMAR N K. Breast cancer prediction model with decision tree and adaptive boosting[J]. IAES International Journal of Artificial Intelligence, 2021, 10(1): 184-190.
[29] NAJI M A, EL FILALI S, AARIKA K, et al. Machine learning algorithms for breast cancer prediction and diagnosis[J]. Procedia Computer Science, 2021, 191: 487-492. doi: 10.1016/j.procs.2021.07.062
[30] AMRANE M, OUKID S, GAGAOUA I, et al. Breast cancer classification using machine learning[C]//2018 Electric Electronics, Computer Science, Biomedical Engineerings' Meeting. Piscataway, NJ: IEEE, 2018: 1-4.
[31] ASSIRI A S, NAZIR S, VELASTIN S A. Breast tumor classification using an ensemble machine learning method[J]. Journal of Imaging, 2020, 6(6): 39. doi: 10.3390/jimaging6060039
[32] KUMARI M, SINGH V. Breast cancer prediction system[J]. Procedia Computer Science, 2018, 132: 371-376. doi: 10.1016/j.procs.2018.05.197
[33] ASRI H, MOUSANNIF H, AL MOATASSIME H, et al. Using machine learning algorithms for breast cancer risk prediction and diagnosis[J]. Procedia Computer Science, 2016, 83: 1064-1069. doi: 10.1016/j.procs.2016.04.224
[34] GHIASI M M, ZENDEHBOUDI S. Application of decision tree-based ensemble learning in the classification of breast cancer[J]. Computers in Biology and Medicine, 2021, 128: 104089. doi: 10.1016/j.compbiomed.2020.104089
[35] NAHATO K B, HARICHANDRAN K N, ARPUTHARAJ K. Knowledge mining from clinical datasets using rough sets and backpropagation neural network[J]. Computational and Mathematical Methods in Medicine, 2015, 2015: 460189.
[36] SAHU B, MOHANTY S, ROUT S. A hybrid approach for breast cancer classification and diagnosis[J]. EAI Endorsed Transactions on Scalable Information Systems, 2019, 6(20): e2.
[37] ALSHAYEJI M H, ELLETHY H, ABED S, et al. Computer-aided detection of breast cancer on the Wisconsin dataset: an artificial neural networks approach[J]. Biomedical Signal Processing and Control, 2022, 71: 103141. doi: 10.1016/j.bspc.2021.103141
[38] ASIF S, WENHUI Y, JINHAI S, et al. A novel one-dimensional convolutional neural network for breast cancer classification[C]//2021 7th International Conference on Computer and Communications. Piscataway, NJ: IEEE, 2021: 847-852.
[39] AGARAP A F M. On breast cancer detection: an application of machine learning algorithms on the Wisconsin diagnostic dataset[C]//Proceedings of the 2nd International Conference on Machine Learning and Soft Computing. New York: ACM, 2018: 5-9.
[40] ABDEL-ZAHER A M, ELDEIB A M. Breast cancer classification using deep belief networks[J]. Expert Systems with Applications, 2016, 46: 139-144. doi: 10.1016/j.eswa.2015.10.015
[41] PEROU C M, SØRLIE T, EISEN M B, et al. Molecular portraits of human breast tumours[J]. Nature, 2000, 406: 747-752. doi: 10.1038/35021093
[42] CASCIANELLI S, MOLINERIS I, ISELLA C, et al. Machine learning for RNA sequencing-based intrinsic subtyping of breast cancer[J]. Scientific Reports, 2020, 10(1): 14071. doi: 10.1038/s41598-020-70832-2
[43] ANDERSON P, GADGIL R, JOHNSON W A, et al. Reducing variability of breast cancer subtype predictors by grounding deep learning models in prior knowledge[J]. Computers in Biology and Medicine, 2021, 138: 104850. doi: 10.1016/j.compbiomed.2021.104850
[44] BUI T D, RAVI S, RAMAVAJJALA V. Neural graph learning: training neural networks using graphs[C]//Proceedings of the Eleventh ACM International Conference on Web Search and Data Mining. New York: ACM, 2018: 64-71.
[45] BINDER A, BOCKMAYR M, HÄGELE M, et al. Morphological and molecular breast cancer profiling through explainable machine learning[J]. Nature Machine Intelligence, 2021, 3(4): 355-366. doi: 10.1038/s42256-021-00303-4
[46] CHEN R P, YANG L, GOODISON S, et al. Deep-learning approach to identifying cancer subtypes using high-dimensional genomic data[J]. Bioinformatics, 2020, 36(5): 1476-1483. doi: 10.1093/bioinformatics/btz769
[47] AGNER S C, ROSEN M A, ENGLANDER S, et al. Computerized image analysis for identifying triple-negative breast cancers and differentiating them from other molecular subtypes of breast cancer on dynamic contrast-enhanced MR images: a feasibility study[J]. Radiology, 2014, 272(1): 91-99. doi: 10.1148/radiol.14121031
[48] ASHRAF A B, DAYE D, GAVENONIS S, et al. Identification of intrinsic imaging phenotypes for breast cancer tumors: preliminary associations with gene expression profiles[J]. Radiology, 2014, 272(2): 374-384. doi: 10.1148/radiol.14131375
[49] HATAMIZADEH A, TANG Y C, NATH V, et al. UNETR: transformers for 3D medical image segmentation[C]//2022 IEEE/CVF Winter Conference on Applications of Computer Vision. Piscataway, NJ: IEEE, 2022: 1748-1758.
[50] CHEN J N, LU Y Y, YU Q H, et al. TransUNet: transformers make strong encoders for medical image segmentationa[EB/ OL]. [2022-08-10]. https://arxiv.org/abs/2102.04306v1.
[51] VALANARASU J M J, OZA P, HACIHALILOGLU I, et al. Medical transformer: gated axial-attention for medical image segmentation[C]//International Conference on Medical Image Computing and Computer-Assisted Intervention. Berlin: Springer, 2021: 36-46.
[52] BENJELLOUN M, ADOUI M E, LARHMAM M A, et al. Automated breast tumor segmentation in DCE-MRI using deep learning[C]//2018 4th International Conference on Cloud Computing Technologies and Applications. Piscataway, NJ: IEEE, 2018: 1-6.
[53] HUO L, HU X X, XIAO Q, et al. Segmentation of whole breast and fibroglandular tissue using nnU-Net in dynamic contrast enhanced MR images[J]. Magnetic Resonance Imaging, 2021, 82: 31-41. doi: 10.1016/j.mri.2021.06.017
[54] CABRERA D L F, GROSSIORD É, GOGIN N, et al. Analysis of lymph node tumor features in PET/CT for segmentation[C]//2021 IEEE 18th International Symposium on Biomedical Imaging. Piscataway, NJ: IEEE, 2021: 588-592.
[55] CABRERA D L F, GOGIN N, MORLAND D, et al. Segmentation of axillary and supraclavicular tumoral lymph nodes in PET/CT: a hybrid CNN/component-tree approach[C]//2020 25th International Conference on Pattern Recognition. Piscataway, NJ: IEEE, 2021: 6672-6679.
[56] AHMED L, IQBAL M M, ALDABBAS H, et al. Images data practices for semantic segmentation of breast cancer using deep neural network[J]. Journal of Ambient Intelligence and Humanized Computing, 2023, 14: 15227-15243. doi: 10.1007/s12652-020-01680-1
[57] SINGH V K, RASHWAN H A, ROMANI S, et al. Breast tumor segmentation and shape classification in mammograms using generative adversarial and convolutional neural network[J]. Expert Systems with Applications, 2020, 139: 112855. doi: 10.1016/j.eswa.2019.112855
[58] 周皓阳, 冯宝, 齐菲菲, 等. 结合MRF能量和DCE-MRI时域特征的乳腺癌灶分割算法[J]. 光子学报, 2021, 50(6): 0610002. https://www.cnki.com.cn/Article/CJFDTOTAL-GZXB202106025.htm ZHOU H Y, FENG B, QI F F, et al. Combining MRF energy and DCE-MRI time-domain features for breast tumors segmentation algorithm[J]. Acta Photonica Sinica, 2021, 50(6): 0610002. (in Chinese) https://www.cnki.com.cn/Article/CJFDTOTAL-GZXB202106025.htm
[59] KEATMANEE C, CHAUMRATTANAKUL U, KOTANI K, et al. Initialization of active contours for segmentation of breast cancer via fusion of ultrasound, Doppler, and elasticity images[J]. Ultrasonics, 2019, 94: 438-453. doi: 10.1016/j.ultras.2017.12.008
[60] DAOUD M I, ATALLAH A A, AWWAD F, et al. Automatic superpixel-based segmentation method for breast ultrasound images[J]. Expert Systems with Applications, 2019, 121: 78-96. doi: 10.1016/j.eswa.2018.11.024
[61] 张旭梅, 范虹, 乔柱. 融合全局和局部信息的水平集乳腺MR图像分割[J]. 计算机应用研究, 2015, 32(1): 307-311. doi: 10.3969/j.issn.1001-3695.2015.01.072 ZHANG X M, FAN H, QIAO Z. Level set method combined global and local information and its application to breast MRI[J]. Application Research of Computers, 2015, 32(1): 307-311. (in Chinese) doi: 10.3969/j.issn.1001-3695.2015.01.072
[62] 虞红伟, 厉力华, 徐伟栋, 等. 一种基于水平集的多尺度乳腺肿块分割方法[J]. 仪器仪表学报, 2010, 31(6): 1418-1423. https://www.cnki.com.cn/Article/CJFDTOTAL-YQXB201006035.htm YU H W, LI L H, XU W D, et al. Multi-scale approach for breast mass segmentation using level set method[J]. Chinese Journal of Scientific instrument, 2010, 31(6): 1418-1423. (in Chinese) https://www.cnki.com.cn/Article/CJFDTOTAL-YQXB201006035.htm
[63] KUO H C, GIGER M L, REISER I, et al. Level set segmentation of breast masses in contrast-enhanced dedicated breast CT and evaluation of stopping criteria[J]. Journal of Digital Imaging, 2014, 27(2): 237-247. doi: 10.1007/s10278-013-9652-1
[64] LIU H, LIU Y P, ZHAO Z W, et al. A new background distribution-based active contour model for three-dimensional lesion segmentation in breast DCE-MRI[J]. Medical Physics, 2014, 41(8): 481-489.
[65] KALLENBERG M, PETERSEN K, NIELSEN M, et al. Unsupervised deep learning applied to breast density segmentation and mammographic risk scoring[J]. IEEE Transactions on Medical Imaging, 2016, 35(5): 1322-1331. doi: 10.1109/TMI.2016.2532122
[66] ROUHI R, JAFARI M, KASAEI S, et al. Benign and malignant breast tumors classification based on region growing and CNN segmentation[J]. Expert Systems with Applications, 2015, 42(3): 990-1002. doi: 10.1016/j.eswa.2014.09.020
[67] ASHRAF A B, GAVENONIS S, DAYE D, et al. A multichannel Markov random field approach for automated segmentation of breast cancer tumor in DCE-MRI data using kinetic observation model[C]//14th International Conference on Medical Image Computing and Computer-Assisted Intervention. Berlin: Springer, 2011: 546-553.
[68] YIN X X, JIAN Y X, ZHANG Y, et al. Automatic breast tissue segmentation in MRIs with morphology snake and deep denoiser training via extended Stein's unbiased risk estimator[J]. Health Information Science and Systems, 2021, 9(1): 16. doi: 10.1007/s13755-021-00143-x
[69] PAREKH V, JACOBS M A. Radiomics: a new application from established techniques[J]. Expert Review of Precision Medicine and Drug Development, 2016, 1(2): 207-226. doi: 10.1080/23808993.2016.1164013
[70] ZHU Y T, LI H, GUO W T, et al. Deciphering genomic underpinnings of quantitative MRI-based radiomic phenotypes of invasive breast Carcinoma[J]. Scientific Reports, 2015, 5: 17787. doi: 10.1038/srep17787
[71] PENG H C, LONG F H, DING C. Feature selection based on mutual information: criteria of max-dependency, max-relevance, and min-redundancy[J]. IEEE Transactions on Pattern Analysis and Machine Intelligence, 2005, 27(8): 1226-1238. doi: 10.1109/TPAMI.2005.159
[72] WANG S, LIU Z Y, RONG Y, et al. Deep learning provides a new computed tomography-based prognostic biomarker for recurrence prediction in high-grade serous ovarian cancer[J]. Radiotherapy and Oncology, 2019, 132: 171-177. doi: 10.1016/j.radonc.2018.10.019
[73] YANG Z N, HE B H, ZHUANG X Y, et al. CT-based radiomic signatures for prediction of pathologic complete response in esophageal squamous cell carcinoma after neoadjuvant chemoradiotherapy[J]. Journal of Radiation Research, 2019, 60(4): 538-545. doi: 10.1093/jrr/rrz027
[74] 高文逸. 脑胶质瘤影像组学特征选择方法研究[D]. 郑州: 郑州大学, 2020. GAO W Y. Feature selection method on glioma for radiomics[D]. Zhengzhou: Zhengzhou University, 2020. (in Chinese)
[75] LI Z H, ZHANG D F, DAI Y G, et al. Computed tomography-based radiomics for prediction of neoadjuvant chemotherapy outcomes in locally advanced gastric cancer: a pilot study[J]. Chinese Journal of Cancer Research, 2018, 30(4): 406-414. doi: 10.21147/j.issn.1000-9604.2018.04.03
[76] LIU Y, KIM J, BALAGURUNATHAN Y, et al. Radiomic features are associated with EGFR mutation status in lung adenocarcinomas[J]. Clinical Lung Cancer, 2016, 17(5): 441-448. doi: 10.1016/j.cllc.2016.02.001
[77] JIA T Y, XIONG J F, LI X Y, et al. Identifying EGFR mutations in lung adenocarcinoma by noninvasive imaging using radiomics features and random forest modeling[J]. European Radiology, 2019, 29(9): 4742-4750. doi: 10.1007/s00330-019-06024-y
[78] YAN M M, WANG W D. Radiomic analysis of CT predicts tumor response in human lung cancer with radiotherapy[J]. Journal of Digital Imaging, 2020, 33(6): 1401-1403. doi: 10.1007/s10278-020-00385-3
[79] MORGADO J, PEREIRA T, SILVA F, et al. Machine learning and feature selection methods for EGFR mutation status prediction in lung cancer[J]. Applied Sciences, 2021, 11(7): 3273. doi: 10.3390/app11073273
[80] 余烨, 吴华伟. 影像组学在肺癌中的应用进展[J]. 国际医学放射学杂志, 2018, 41(6): 646-649. https://www.cnki.com.cn/Article/CJFDTOTAL-GWLC201806007.htm YU Y, WU H W. Application progress of radiomics in lung cancer[J]. International Journal of Medical Radiology, 2018, 41(6): 646-649. (in Chinese) https://www.cnki.com.cn/Article/CJFDTOTAL-GWLC201806007.htm
[81] SONG J, DING C, HUANG Q, et al. Deep learning predicts epidermal growth factor receptor mutation subtypes in lung adenocarcinoma[J]. Medical Physics, 2021, 48(12): 7891-7899. doi: 10.1002/mp.15307
[82] MU W, JIANG L, ZHANG J Y, et al. Non-invasive decision support for NSCLC treatment using PET/CT radiomics[J]. Nature Communications, 2020, 11: 5228. doi: 10.1038/s41467-020-19116-x
[83] WANG H Z, SUBRAMANIAN V, SYEDA-MAHMOOD T. Modeling uncertainty in multi-modal fusion for lung cancer survival analysis[C]//2021 IEEE 18th International Symposium on Biomedical Imaging. Piscataway, NJ: IEEE, 2021: 1169-1172.
[84] YAMAMOTO S, MAKI D D, KORN R L, et al. Radiogenomic analysis of breast cancer using MRI: a preliminary study to define the landscape[J]. American Journal of Roentgenology, 2012, 199(3): 654-663. doi: 10.2214/AJR.11.7824
[85] LIU C L, DING J, SPUHLER K S, et al. Preoperative prediction of sentinel lymph node metastasis in breast cancer by radiomic signatures from dynamic contrast-enhanced MRI[J]. Journal of Magnetic Resonance Imaging, 2019, 49(1): 131-140. doi: 10.1002/jmri.26224
[86] WANG X X, ZOU C, ZHANG Y, et al. Prediction of BRCA gene mutation in breast cancer based on deep learning and histopathology images[J]. Frontiers in Genetics, 2021, 12: 661109. doi: 10.3389/fgene.2021.661109
[87] MAZUROWSKI M A, ZHANG J, GRIMM L J, et al. Radiogenomic analysis of breast cancer: luminal B molecular subtype is associated with enhancement dynamics at MR imaging[J]. Radiology, 2014, 273(2): 365-372. doi: 10.1148/radiol.14132641
[88] LIU J, WU Y R, ONG I, et al. Leveraging interaction between genetic variants and mammographic findings for personalized breast cancer diagnosis[C]//AMIA Summits on Translational Science Proceedings. Bethesda, MD: AMIA, 2015: 107-111.
[89] SUN Q C, LIN X N, ZHAO Y S, et al. Deep learning vs. radiomics for predicting axillary lymph node metastasis of breast cancer using ultrasound images: don't forget the peritumoral region[J]. Frontiers in Oncology, 2020, 10: 53. doi: 10.3389/fonc.2020.00053
[90] LIU T, HUANG J, LIAO T, et al. A hybrid deep learning model for predicting molecular subtypes of human breast cancer using multimodal data[J]. Innovation and Research in Biomedical Engineering, 2022, 43(1): 62-74.
[91] LIN P, LIU W K, LI X, et al. MRI-based radiogenomics analysis for predicting genetic alterations in oncogenic signalling pathways in invasive breast carcinoma[J]. Clinical Radiology, 2020, 75(7): 561. e1-561. e11. doi: 10.1016/j.crad.2020.02.011
[92] ZHU B Y, LUO W, LI B P, et al. The development and evaluation of a computerized diagnosis scheme for pneumoconiosis on digital chest radiographs[J]. BioMedical Engineering OnLine, 2014, 13: 141. doi: 10.1186/1475-925X-13-141
[93] ZHANG L F, FRIED D V, FAVE X J, et al. IBEX: an open infrastructure software platform to facilitate collaborative work in radiomics[J]. Medical Physics, 2015, 42(3): 1341-1353. doi: 10.1118/1.4908210
[94] SZCZYPIUSKI P M, STRZELECKI M, MATERKA A, et al. MaZda—a software package for image texture analysis[J]. Computer Methods and Programs in Biomedicine, 2009, 94(1): 66-76. doi: 10.1016/j.cmpb.2008.08.005
[95] MAYERHOEFER M E, SCHIMA W, TRATTNIG S, et al. Texture-based classification of focal liver lesions on MRI at 3.0 Tesla: a feasibility study in cysts and hemangiomas[J]. Journal of Magnetic Resonance Imaging, 2010, 32(2): 352-359. doi: 10.1002/jmri.22268
[96] BASU S, HALL L O, GOLDGOF D B, et al. Developing a classifier model for lung tumors in CT-scan images[C]//2011 IEEE International Conference on Systems, Man, and Cybernetics. Piscataway, NJ: IEEE, 2011: 1306-1312.
[97] 李双双, 侯震, 刘娟, 等. 影像组学分析与建模工具综述[J]. 中国医学物理学杂志, 2018, 35(9): 1043-1049. doi: 10.3969/j.issn.1005-202X.2018.09.010 LI S S, HOU Z, LIU J, et al. Review of radiomic analysis and modeling tools[J]. Chinese Journal of Medical Physics, 2018, 35(9): 1043-1049. (in Chinese) doi: 10.3969/j.issn.1005-202X.2018.09.010
[98] JIANG Y Z, LIU Y, XIAO Y, et al. Molecular subtyping and genomic profiling expand precision medicine in refractory metastatic triple-negative breast cancer: the FUTURE trial[J]. Cell Research, 2021, 31: 178-186. doi: 10.1038/s41422-020-0375-9
[99] YANG F, XIAO Y, DING J H, et al. Ferroptosis heterogeneity in triple-negative breast cancer reveals an innovative immunotherapy combination strategy[J]. Cell Metabolism, 2023, 35(1): 84-100. doi: 10.1016/j.cmet.2022.09.021
[100] TOǦAÇR M, ÖZKURT K B, ERGEN B, et al. BreastNet: a novel convolutional neural network model through histopathological images for the diagnosis of breast cancer[J]. Physica A: Statistical Mechanics and Its Applications, 2020, 545: 123592. doi: 10.1016/j.physa.2019.123592
[101] KHAN S I, SHAHRIOR A, KARIM R, et al. MultiNet: a deep neural network approach for detecting breast cancer through multi-scale feature fusion[J]. Journal of King Saud University-Computer and Information Sciences, 2022, 34(8): 6217-6228. doi: 10.1016/j.jksuci.2021.08.004
[102] LIM T S, TAY K G, HUONG A, et al. Breast cancer diagnosis system using hybrid support vector machine-artificial neural network[J]. International Journal of Electrical and Computer Engineering, 2021, 11(4): 3059-3069.
[103] MEHMOOD M, AYUB E, AHMAD F, et al. Machine learning enabled early detection of breast cancer by structural analysis of mammograms[J]. Computers, Materials & Continua, 2021, 67(1): 641-657.



 下载:
下载: